クロストリディオイデス(クロストリジウム)・ディフィシル: Clostridioides(Clostridium) difficileは、一部の健常者の腸内に定着する常在菌の一種です。
通常は、ほかの腸内細菌により、増殖が抑制されていますが、抗菌薬を投与した場合の副作用として、生命を脅かす下痢を引き起こすことがあります。
抗菌薬の投与により、正常な腸内細菌叢が撹乱されると、異常増殖して毒素を産生し、下痢症を引き起こします。抗生物質の投与を開始してから数日または数週間以内に症状が現れることがあります。
C.difficile が形成する芽胞は、過酷な環境でも安定で、アルコール耐性があり、多くの抗菌薬に対しても抵抗性があります(経口感染するため、院内感染対策上、重要な菌)。
クロストリディオイデス(クロストリジウム)・ディフィシル: Clostridioides(Clostridium) difficile
クロストリディオイデス(クロストリジウム)・ディフィシル: Clostridioides(Clostridium) difficileは、グラム陽性偏性嫌気性細菌です。
酸素の存在下では発育することが困難です。
1935年に健常新生児の糞便から分離されたのが最初です。
その後1978年に抗菌薬関連の偽膜性大腸炎(pseudomembranous colitis)の原因菌として報告されました。
C. difficileの主たる病原因子は、トキシンA,トキシンB,バイナリ―トキシンという3種類の毒素が確認されている。
感染経路
腸内に定着した常在性のC.difficileによるもののほかに、保菌健常者やCDAD発症者の糞便を介した接触感染が主な感染経路です。
C. difficileは、芽胞形成性のグラム陽性偏性嫌気性細菌であるため、形成された芽胞が長期間にわたって環境中に生残し、それが院内感染や再発の感染源となる場合があります。
C. difficileには、毒素産生株と毒素非産生株とが存在します。毒素産生株が、健常者に定着することもあり、検出時に定着しているだけなのかを判断するのは簡単ではありません。
発症まで
クロストリディウム・ディフィシルは、通常は、他の腸内細菌により増殖が抑制されています。
しかし、広域スペクトルの抗菌薬の投与により、大腸菌をはじめとする腸内細菌が死滅して腸内フローラ環境が破壊されると、クロストリディウム・ディフィシルが異常増殖をきたします。
クロストリディウム・ディフィシルは、毒素(トキシンAおよびトキシンBなど)を産生し、C.difficile関連下痢症(CDAD;CDIとも)を引き起こします。
CDI診療ガイドラインでは、24時間以内に3回以上もしくは平常時よりも多い便回数の下痢を生じ、糞便中のCDI検査で毒素陽性もしくは毒素産生性C. difficileを認めるか、内視鏡検査で偽膜性腸炎像を認めるものをCDIと定義しています。
診断
診断は、消化器症状に加えて酵素抗体法(トキシンAとトキシンBの同時検出キット)で確定診断となります。
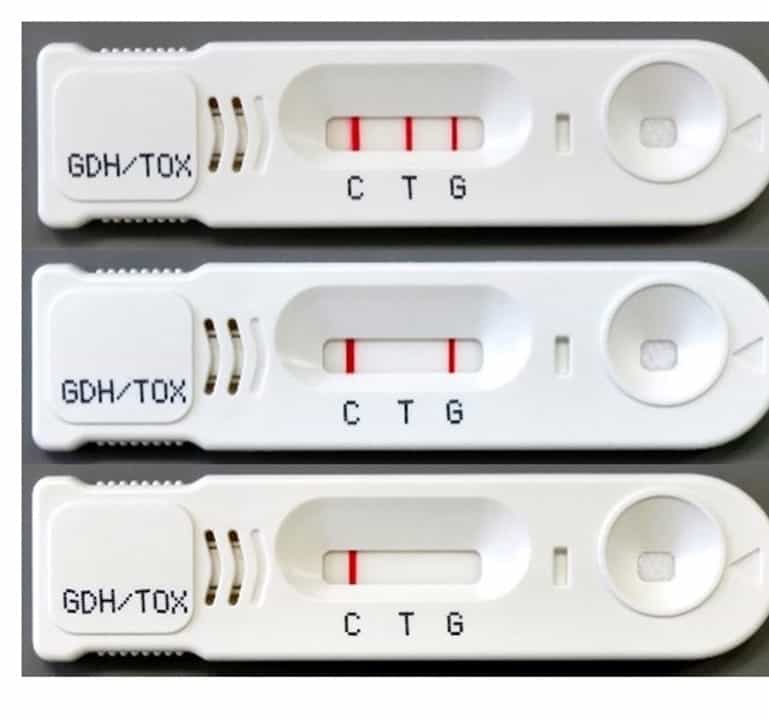
上記の検査キットの添付文書では、CD抗原の感度は 88~94%、特異度は 89~94%。、CD毒素の感度は 73~87%,特異度は 97~98%と紹介されています。
また、ポリメラーゼ連鎖反応(PCR)やLoop-Mediated Isothermal Amplification(LAMP)法を用いた糞便中毒素遺伝子検査法(Nucleic Acid Am- plification Test:NAAT)を利用することができます。
PCRを使う場面は、上記の検査キットにて、抗原のみ(+)の場合です。上記の検査キットだけしか使えない状況では、感度を上げるため、C.difficileを培養してから、検査キットに菌液を滴下し、毒素の産生の有無を再検査をしていました(二段階法)。これは、判定まで、最長で2日を要します。しかし、PCR検査であれば、便検体から、直接にCD毒素遺伝子を検出できるため、即日判定が可能です(そのうえ高感度かつ高特異度)。しかも、機器によっては、バイナリートキシンを検出できるものがあります(ジーンエキスパート:GeneXpert ®など)。
なお、病原性を示すにはtoxin Bの産生が必須であることが動物モデルによって示されています。
毒素陰性でNAAT陽性の場合には,少量の毒素産生株の定着である可能性も考慮に入れて診断する必要があります。
培養については、特殊な培地を用います。便からC.difficileを発育させるには、サイクロセリンとセフォキシチンを含有する培地を使用する必要があります。サイクロセリン・セフォキシチン・マニトール寒天培地(CCMA寒天培地)、あるいは、サイクロセリン・セフォキシチン・フルクトース寒天培地(CCFA寒天培地)を使用します。
治療
治療としては、まず脱水を補正します。
そして、経腸栄養、化学療法、下剤など、他の下痢を来す原因を除外します。
なお、経腸栄養剤投与時の下痢の原因には、つぎのものがあり、CD腸炎(CDI)も含まれます。
- 投与速度:投与速度が速すぎる
- 栄養剤の浸透圧(高浸透圧性の下痢)
- 栄養剤の組成(乳糖不耐症,食物繊維の不足など)
- 細菌汚染(長すぎる投与時間:8時間以上)
- 温度(冷たい栄養剤は腸管を刺激して下痢を誘発する恐れ)
- ソルビトール含有薬剤や消化管運動促進剤などの薬剤投与
- 短腸症候群や炎症性腸疾患などの病態の合併
- CD腸炎の合併
原因抗菌薬を中止し、バンコマイシンまたはメトロニダゾールの経口投与が有効です。
プロバイオティクスの投与も有効との報告もあります。
なお、CDトキシン検査が陰性でも、抗菌薬使用中または使用歴があり、下痢を来す他の原因がはっきりしない場合は、治療を検討すべきです。
PPIとCDI発症リスク
経腸栄養やプロトンポンプ阻害薬(PPI) により、CDIの発症リスクが上昇するという話があります。
- PPI(ランソプラゾールなど)の添付文書には次の記載があります。「海外における主に入院患者を対象とした複数の観察研究で、プロトンポンプインヒビターを投与した患者においてクロストリジウム・ディフィシルによる胃腸感染のリスク増加が報告されている。」
- PPIにより胃内のpHが上昇することで、胃酸によるC.difficile の殺菌力が低下し、 C.difficileの腸内細菌叢への定着が容易になるという説があります。
また、多くのCDI患者は見過ごされている可能性があることが指摘されています。
https://www.facebook.com/NTMC.AST/posts/652355061849637/ では、つぎのように記載されています(引用)。
国立感染症研究所の加藤はる先生と多摩総合医療センターの本田仁先生らを中心に、東京医療センターを含めた全12施設(20病棟)が参加して行われた研究がpublishされました。(参加施設:八戸市立市民病院、亀田総合病院、東京ベイ浦安市川医療センター、東京医療センター、豊川市民病院、東海中央病院、奈良県立医科大学附属病院、刀根山病院、呉医療センター・中国がんセンター、下関市立大学市民病院、産業医科大学病院、沖縄県立南部医療センター)
Bristol stool scale 6-7の便を3回/24h以上認めた患者さんのC.difficileのトキシン、培養検査、遺伝子検査を施行。・全体のCDI発生率 7.41/10,000患者・日。ICU(5病棟)では22.2/10,000患者・日・全体のCDI検査頻度は、30.36/10,000患者・日・CDI検査頻度とCDI発生率は高い相関関係にある(R2=0.91)・分離したPCRリボタイプは018(29%)、014(23%)、002(12%)、369(11%)。過去の日本の報告と比べて発生率は高い結果となっており、これまでのCDI発症率は過小評価されていた可能性があります。
以上、ご参考まで。