定義
アンチバイオグラムとは、細菌ごとの抗菌薬感受性率表のことです。
解説
病院などの施設では、微生物検査室が、検体から検出された菌に対して、どのような薬が効果があるのかを検証しています(感受性試験;antimicrobial susceptibility test data;antimicrobial susceptibility testing)。
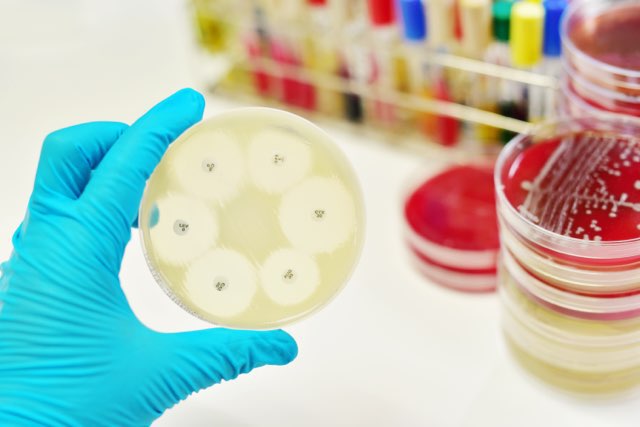
なお、検証方法には、ディスク拡散法や、微量液体希釈法、Etest®などがあります。
その結果を基に、薬に対する感受性を、S(感性)、I(中間)、あるいはR(耐性)で判定し、臨床側に提供しています。
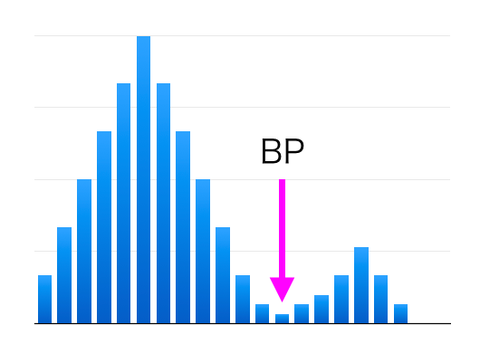
S、I、Rの判定基準は、CLSI(Clinical and Laboratory Standards Institute、臨床・検査標準協会)の設定した基準(ブレイクポイント:BP)が用いられることがほとんどで、一部、日本化学療法学会(JSC)の設定するBPを用いる施設もあります。
また、施設によっては、EUCAST(European committee on Antimicrobial Susceptibility Testing)の設定したBPを用いて、S(有効)、I(中間)あるいはR(無効)で判定しています。
その判定結果を、施設ごとに(施設によっては更に診療科ごとに)、統計処理してまとめた表が、アンチバイオグラムです。
この表では、特定の菌種が、抗菌薬に対し、S(感性/有効)、I(中間)、またはR(耐性/無効)を示す確率(%)を記載しています。
たとえばの話ですが、新規外来患者を対象に実施した細菌検査において、一定期間の間に、黄色ブドウ球菌を100検体から検出した場合に、そのうちの95菌株がアルベカシン(ABK)にS(感性)を示し、4菌株がI(中間)を示し、1菌株がR(耐性)を示したとすれば、Sは95%、Iは4%、Rは1%と記載されます。
アンチバイオグラムを見れば、検出菌の同定試験の結果が報告された後から感受性試験の結果が報告される前までの間に、有効な抗菌薬を選択したり、投与計画を練ったりするための有用な参考情報となります。
とくに、第三世代セフェムや、カルバペネムなどの広域スペクトルの抗菌薬から、狭域スペクトルの薬に変更するとき(デ・エスカレーション)の参考情報となる点がメリットです。
アンチバイオグラムを参考に、より効果の高い抗菌薬に変更することで早期に治療が完了したり、耐性菌の出現を抑制したりすることが可能です。加えて、より安価な薬に変更できれば、医療費を下げることもできます。
つまり、アンチバイオグラムを用いて治療すれば、従来の経験的治療(エンピリック治療、エンピリックセラピーとも呼ばれる)に比べて、適切な抗菌薬を選べる確率が高まります。
さらに、毎年のアンチバイオグラムを作成することによって、薬剤耐性菌の動向を把握することもできます。
なお、近年は、質量分析装置(MALDI/TOFMS)や遺伝子検査により迅速に菌名が同定できる環境が整い、敗血症などの重症例にアンチバイオグラムが極めて大きな貢献をするようになりました。
課題
施設間でアンチバイオグラムを比較すること、ならびに、地域レベルのアンチバイオグラムを作成することに難しさがあります。
その原因は、アンチバイオグラムを作成するときのデータの抽出方法です。
ひとりの患者の複数部位から同一菌種が検出された場合の処理方法や、治療後に一定期間経過した後に同じ菌が患者(特に入院患者)から検出された場合の処理方法などに、色々な考え方があり、施設ごとに採用している方法が、完全に同一ではないためです。
よって、地域の施設間で、アンチバイオグラムを作成する際の統計処理方法を統一することが重要と言われています。
なお、CLSIは、アンチバイオグラムの作成方法に関し、ガイドラインを打ち出しています。