梅毒の概要
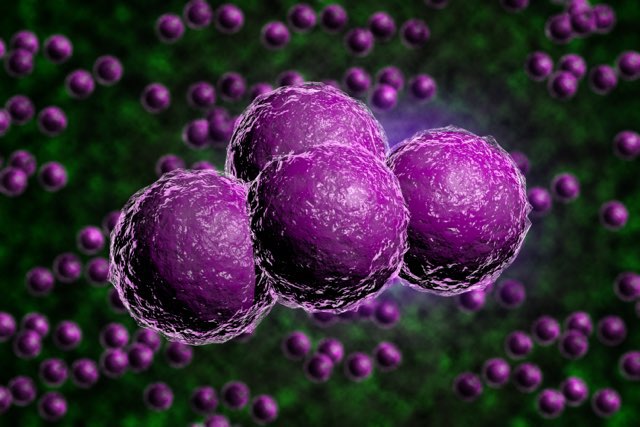
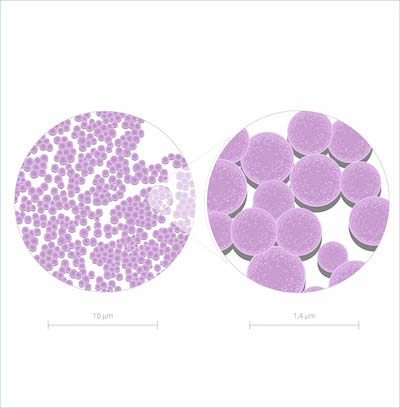
梅毒はスピロヘータ目に属する梅毒トレポネーマ Treponema pallidum subsp. pallidum(直径0.1〜0.2μm、長さ10〜20μmのらせん状菌)により生じる性感染症です。
梅毒は、性感染症のひとつですが、まれに接触感染や輸血による感染もあります。
胎児が母体内で経胎盤的に感染する場合があり、これは「先天梅毒」と呼ばれ、妊娠中の女性における積極的な診断と治療は先天梅毒を防ぐために特に重要とされます。
それ以外の感染症は、「後天梅毒」と呼ばれます。
なお、皮膚や臓器での梅毒による症状がみられるものを「顕性梅毒」とし、症状はみられないが梅毒血清反応が陽性であるものを「無症候梅毒」という区別もあります。
感染のメカニズムとしては、皮膚や粘膜の微小な傷から梅毒トレポネーマが侵入して感染し、局所で増殖した後、やがて血行性に全身に散布されて種々の症状を引き起こします。
なお、梅毒は日本の感染症法で5類感染症です。
患者や、無症状であっても病原体を保有する者について、全例を都道府県知事に届け出る必要があります。
臨床像(症状)
後天梅毒では、臨床像は、第一期梅毒(早期の顕症梅毒)、第二期梅毒、無症候性の潜伏期梅毒(第三期梅毒)、第四期梅毒(晩期顕症梅毒)に大別されます。
第一期梅毒
第一期梅毒は、感染後平均3週間で発症します。
早い場合は3〜10日程度、遅い場合は90日程度と幅があります。
男性の陰茎亀頭部や女性の陰唇部に発症します。
トレポネーマの侵入部位である感染局所に無痛の硬結が生じ(初期硬結)、周囲は隆起し中心部に潰瘍を形成して下疽(げかん)となります。
また局所所属リンパ節腫脹が認められます。
第二期梅毒
第二期梅毒は、トレポネーマが血行性に全身播種し、主に上皮表面を障害します。
そのため、皮疹などの身体所見や発熱倦怠感、鼻汁、咽頭痛、筋肉痛、頭痛、圧痛のない全身性リンパ節腫脹などの全身徴候が認められます。
第二期梅毒は、第一期梅毒後2〜12週間、長い場合には6ヶ月後までの問に発症します。
第二期梅毒では、主に皮膚が障害され、大半の事例で、皮疹あるいは粘膜疹が認められます。
初期には全身性の掻痒を伴わない斑状発疹あるいは紅斑が体幹から生じ肩から四肢に広がり2週間程度認められます(通常手掌や足底顔面にはみられない)。
典型的な皮疹は「バラ疹」と呼ばれます。
潜伏期梅毒
第二期梅毒が無治療の場合や、第四期梅毒を発症するまで、ある程度の期間潜在性に無症候で経過をする時期があります。
この期間は「潜伏期梅毒」呼ばれます。
潜伏期梅毒は最初の1年間に粘膜病変が再発し、感染性のリスクが高い状況になります。
第四期梅毒
第四期梅毒は大きく、心血管梅毒と神経梅毒に分かれます。
心血管梅毒のうち、「梅毒性大動脈炎」は未治療梅毒の70~80%に生じると言われています。
また、合併症(大動脈の循環不全や動脈瘤、冠動脈入口部狭窄など)は、初感染の10~20年後、未治療梅毒の10~15%に生じます。
なお、動脈瘤形成は梅毒性大動脈炎の中でも稀であり5~10%に生じると言われます。
多くは単一の動脈瘤であり,紡錘状よりは嚢状のことが多く、50%は上行大動脈に生じ、大動脈弓部の病変は上行大動脈についで頻度が高く30~40%です。
食道、気管、左気管支、左反回神経に接していることから、疾痛、呼吸困難咳、嗅声、嚥下障害などの症状を比較的早期に呈すると言われています。
検査
病原体の培養が不可能なため、診断は臨床症状にくわえて、病理所見、血清所見によります。
すなわち、梅毒を診断する方法には、病変からトレポネーマを顕微鏡などで直接確認する方法と、血清学的な検査方法があります。
顕微鏡検査では、初期硬結や硬性下疽の表面をメスで擦過して得た液体をスライドグラスに採取し、ブルー・ブラックインク(パーカー社製)、ギムザ液、または墨汁を混ぜて薄くのばし、乾燥後に、顕微鏡の油浸で観察または暗視野顕微鏡により観察します。
血清学的検査は、非トレポネーマ検査と、特異的トレポネーマ検査とが主に用いられます。
非トレポネーマ検査
非トレポネーマ検査はリン脂質のカルジオリピン抗原に対する抗体価を測定するserologic test for syphilis(STS)法で, rapid plasma regain card test(RPR)法とラテックス凝集法が頻用されています。
梅毒感染後2~4週間で陽性となり、通常第二期梅毒から早期潜伏梅毒にかけて最も高くなります。
疾病の活動性と相関することが多いものの、妊婦や高齢者、膠原病、慢性肝疾患、結核、HIV感染などがあると疑陽性となることがあるため(生物学的偽陽性反応:biological false positive:BFP)、結果の解釈に注意が必要です。
STS法は梅毒の治療を開始すると値は低下するが、十分な治療を行っても抗体価が陰性にならない場合もあります(serofast reaction)。
特異的トレポネーマ検査
特異的トレポネーマ検査はT.pallidumの菌体成分に対する反応を測定する方法(TP抗原法)で、Treponema Pallidum Hemagglutination Test(TPHA)法、Fuorescent treponemal antibody absorption test(FTA-ABS)法、ラテックス凝集法、venereal disease research laboratry(VDRL)があります。
特異的トレポネーマ検査は、通常は非トレポネーマ抗体検査が陽性となってから2~3週間後に遅れて陽性となります。
特異的トレポネーマ検査は、非トレポネーマ抗体検査とは異なり疾患特異性が高く、陽性の場合にはこれまでに梅毒に曝露されたことを示します。
ゆえに、特異的トレポネーマ検査は確定診断には必須です
ただし、特異的トレポネーマ検査は、非トレポネーマ抗体検査のように疾患活動性とは相関せず、治療によってT.pallidumが消失した後も陽性が持続しますので、治療効果判定には使用されません。
FTA-ABS抗体のうちIgM抗体は初感染後1週間で産生され約1ヶ月でピークに達し、その頃からIgG抗体が産生されはじめ,3ヶ月頃にピークに達するため、これらを組み合わせることでより正確な診断が可能となります。
RPR、TP抗体ともに陰性は梅毒非感染、RPR陽性/TP抗体陰性およびRPR陰性/TP抗体陽性はガラス板法で再確認を必要とし、RPR陽性/TP抗体陽性例は梅毒感染として解釈できます。
治療
病期にかかわらず、ペニシリンが常に選択されるべき抗菌薬です。
用量・期間・投与経路が病期によって異なります。
国際的には、第一期・第二期梅毒に対し、ベンザチンペニシリン筋注の使用が推奨されています。
心血管梅毒・神経梅毒に対してはベンジルペニシリン静注を用います。
ペニシリン以外の抗菌薬の有効性は、ペニシリンに劣るか、または不明とされています。
可能な限りペニシリンを使用します。
なお、 妊婦の治療は垂直感染の予防を考慮し妊娠週数にかかわらず治療を開始します。
ペニシリン系薬は妊婦にも投与可能である。
ペニシリンアレルギーの場合は脱感作を行って投与を試みることが推奨されます。